La cella ad idrogeno diventa ecocompatibile
E' stato scoperto il funzionamento degli enzimi idrogenasi, che permette così di sviluppare nuove tecnologie ecocompatibili per utilizzare l'idrogeno come combustibile.
Ma cosa sono le idrogenasi? sono degli enzimi "che catalizzano l'ossidazione reversibile dell'idrogeno molecolare". In natura sono presenti in alghe e batteri, che li "utilizzano per trasformare l'energia chimica contenuta nella molecola di idrogeno e renderla un alimento". Ed ecco che quello che viene fatto dagli esseri in natura, spesso fa comprendere all'uomo che quello stesso meccanismo potrebbe riuscire a ricrearlo lui stesso. In questo caso si tratta di sfruttare l'idrogeno come combustibile, creando delle celle che si comportino allo stesso modo.
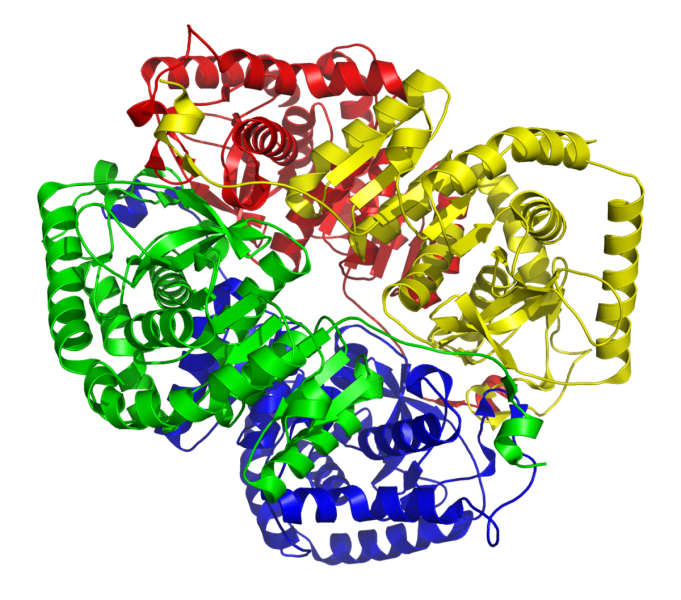
(Un modello degli enzimi idrogenasi)
Gli studi sono stati portati avanti dall'Università di Milano-Bicocca ed altre facoltà europee e la scoperta è stata pubblicata sulle riviste Nature Chemistry e Journal of the American Chemical Society. Questa ricerca ha svelato alcune caratteristiche della struttura degli enzimi idrogenasi, che fino ad ora erano rimaste sconosciute. Portando così alla luce i meccanismi che si trovano alla base dell'attività catalitica.
"Scoprire la struttura e il meccanismo di funzionamento delle idrogenasi - dicono da Milano Bicocca - rappresenta una delle possibili chiavi di volta per la progettazione di celle a combustibile a basso costo, dal momento che quelle attualmente disponibili sul mercato necessitano della presenza di palladio o platino, più costosi del ferro e del nichel utilizzati negli studi. A livello di tempistiche, stiamo parlando di un possibile sviluppo nell'arco di quattro-cinque anni". Il contributo essenziale ruota intorno alla comprensione della reazione grazie alla quale "le ferro-idrogenasi si proteggono dall'ossigeno molecolare evitando così di arrugginirsi e smettere di funzionare". Gli ioni di nichel saranno probabilmente utilizzati per creare le celle a combustibile, nei prossimi anni, quando saranno portati avanti ulteriori sviluppi.
Il sito attivo dell'enzima ha delle caratteristiche di flessibilità inattese, alla base della sua robustezza, infatti "i componenti del sito attivo dell'enzima mostrano un grado di mobilità notevole, che consente all'enzima di interagire con l'idrogeno in maniera anche non convenzionale, evitando così processi potenzialmente distruttivi per la proteina".
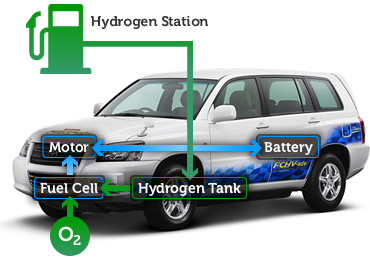
(Una quantità minima di proteine ferro-idrogenasi potrebbero fare il pieno al serbatoio di una macchina alimentata ad idrogeno)
Lo studio che è stato elaborato in maniera più teorica dalla Milano-Bicocca è stato invece praticamente analizzato sul campo dall'Università Humboldt di Berlino, che ha sintetizzato una molecola innovativa, che ha la capacità di legare e trasformare l'acido formico, che è sicuramente più facile da immagazzinare rispetto all'idrogeno.
Una piccola quantità di proteina ferro-idrogenasi sarebbe in grado di riempire il serbatoio di un automobile alimentata ad idrogeno, in quanto una sola molecola può generare 9.000 molecole di idrogeno al secondo. Ovviamente, quello che si dovrebbe cercare di fare è avere una produzione che possa competere su scala industriale. E' stato comunque fatto un passo avanti decisivo, per la progettazione futura di catalizzatori sintetici, che siano in grado di lavorare come quelli naturali.
Una delle poche società che punta alla produzione di macchine ad idrogeno in un periodo a breve tempo è la Toyota, la quale vorrebbe immettere nel mercato dell'anno prossimo la Toyota FCV, che grazie alle celle a combustibile che reagiscono con l'ossigeno, alimentano il motore elettrico.











